빅파마들, 이중항체 관련 대규모 딜 적극 체결... 이중항체 시장 본격화
에이비엘바이오, 이뮨온시아, 파멥신의 이중항체, 국가신약개발 과제 선정

[바이오타임즈] 연간 1조 원 이상 매출을 올릴 수 있는 글로벌 신약 개발을 목표로 하는 ‘국가신약개발사업’의 신규 선정 과제가 속속 발표되고 있다.
해당 사업은 블록버스터 신약 개발을 위해 관계부처 간 연구개발 역량을 총결집하는 범부처 국가 R&D사업으로, 올해 7월부터 향후 10년간 총 2조 2,000억 원을 투입한다.
국가신약개발사업단(KDDF, 단장 묵현상)은 미국 식품의약국(FDA)과 유럽의약품청(EMA)의 신약 승인 4건과 글로벌 기술이전 60건 등을 목표로 향후 10년간 유효·선도물질과 후보물질을 발굴하고, 비임상, 임상 1·2상, 사업화 등의 신약 개발 사업을 지원한다.
◇이중항체 의약품, 기존 병용요법 단점 해결로 관심 증가
최근 국가신약개발 과제에 선정된 항암 신약의 라인업을 보면 이중항체 항암제가 대세로 떠오르고 있음을 알 수 있다. ‘이중항체’란 하나의 항체가 서로 다른 2개의 항원에 결합하도록 하는 항체 단백질로, 단일항체가 질병을 유발하는 1개의 인자를 인식하는 것과 달리 이중항체는 2개 이상의 인자에 작용하기 때문에 효능이 우수하다.
이에 이중항체 의약품은 기존 병용투여법의 단점을 해결할 수 있는 대책으로 업계의 관심을 받고 있다. 최근 이중항체 면역항암제 임상 건수가 증가하고 있으며, 글로벌 빅파마 역시 이중항체 관련 대규모 딜을 적극적으로 체결하면서 이중항체 시장이 본격화되고 있다.
의약품 시장 조사기업 루츠 애널리시스에 따르면 글로벌 이중항체 의약품 시장 규모도 2017년 1억 8,000만 달러(약 2,000억 원)에서 연평균 34% 성장해 2030년 90억 달러(약 10조 원)로 성장할 전망이다.
◇에이비엘바이오, 이뮨온시아, 파멥신의 이중항체, 국가신약개발 과제 선정
항체치료제 개발 전문 기업 파멥신(208340, 대표이사 유진산)은 최근 PD-L1과 SIRPα를 타깃하는 이중표적 항체치료제 연구개발(R&D)이 국가신약개발사업단의 ‘신약 기반 확충연구’과제에 선정됐다고 지난 13일 밝혔다.
PD-L1과 T세포 표면에 있는 PD-1 수용체의 상호작용은 암세포 사멸을 억제하는 반면, 식세포의 표면 SIRPα 수용체에 대한 CD47의 결합은 암세포 제거를 억제하는 것으로 알려졌다. 파멥신은 이러한 점에 착안해 PD-L1뿐만 아니라 암세포들의 면역 회피 기능과 연관된 SIRPα/CD47을 동시에 표적함으로써 암세포의 식균 작용과 생체 내 항종양 면역 반응 향상을 높이는 이중항체 기반의 약물을 개발할 방침이다.
특히 SIRPα/CD47 결합 항체는 PD-1/PD-L1 병용투여 후보 물질로 글로벌 빅 파마들의 주목을 받고 있다. 실제로 올해 8월 SIRPα 파이프라인을 보유한 면역항암제 전문 제약기업이 화이자에 약 22.6억 달러(2조 6,000억 원)에 인수된 바 있다.
면역항암제 전문기업 이뮨온시아(대표 김흥태)는 이중항체 ‘IOH-001’의 전임상 연구가 국가신약개발사업단의 ‘신약 R&D 생태계 구축 연구-비임상’ 부문 신규 과제로 선정됐다고 21일 밝혔다.
이번 선정으로 이뮨온시아는 ‘IOH-001”의 임상시험계획서(IND) 제출 및 승인까지 2년간 연구개발비를 지원받는다.
이뮨온시아는 유한양행과 나스닥 상장사인 미국의 소렌토 테라퓨틱스가 합작하여 설립한 면역항암제 전문 신약개발 기업이다. 지난 3월에는 중국 3D메디슨에 CD47 항체 후보물질인 ‘IMC-002’의 중국지역 개발권리를 총 5,400억 원에 기술이전하는 계약을 체결했다.
이뮨온시아가 개발한 ‘IOH-001(PD-L1xCD47 이중항체)’은 IMC-001(PD-L1항체)을 Base Asset으로 활용해 독자적으로 개발했다. 암세포에 발현되는 PD-L1 및 CD47을 동시에 표적함으로써 선천면역과 후천면역을 동시에 활성화해 난치성 암에서도 높은 효과를 보일 것으로 기대된다.
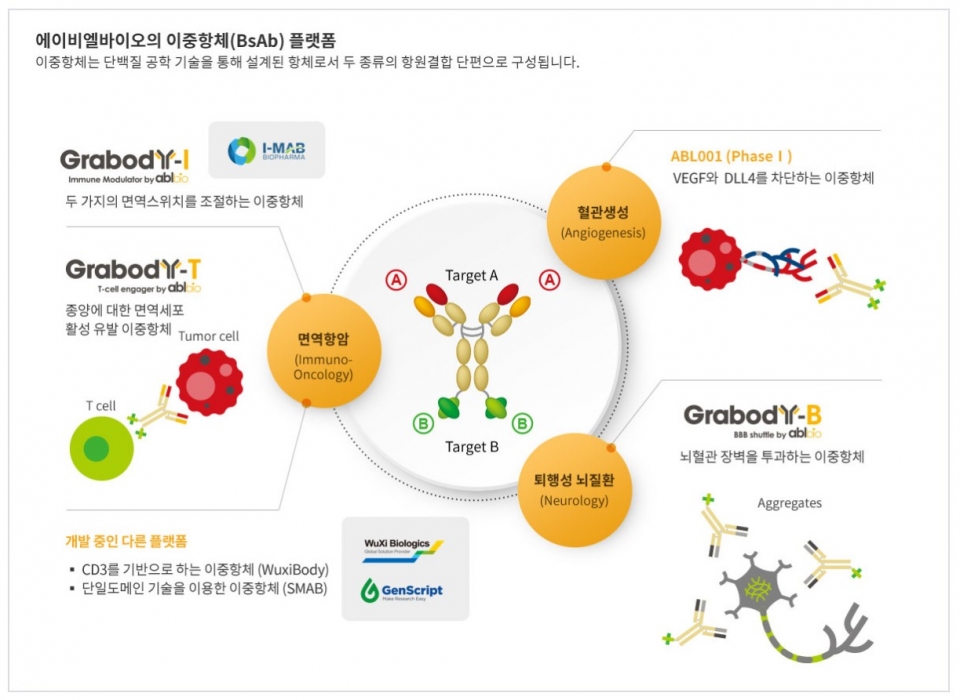
이중항체 전문기업 에이비엘바이오(대표 이상훈, 298380)는 면역항암 이중항체 후보 물질 ABL501이 정부의 국가신약개발사업 신약 임상 개발 과제로 선정돼, 2021년 11월부터 24개월간 임상 1상 진행을 위한 연구개발비를 지원받게 된다고 21일 밝혔다.
에이비엘바이오는 이번 과제를 통해 ABL501의 단독용량증량시험(1a상)과 병용증량시험(1b상)을 완료하고, 2023년 임상 2상 시험계획서(IND) 신청 등의 단계에 돌입할 예정이다.
ABL501은 이중항체 플랫폼 ‘그랩바디-I(Grabody-I)’ 기술을 활용한 고형암 치료제 후보물질로, 두 가지 서로 다른 종류의 면역관문 단백질인 LAG-3와 PD-L1을 타깃으로 한다. LAG-3 항체는 T세포의 종양 살상기능을 회복시킴으로써 기존 면역관문억제제의 반응률을 높여 환자들의 관해(Remission) 달성을 유도한다. BMS(Bristol Myers Squibb)가 흑색종 환자 대상 LAG-3 항체 렐라틀리맙(Relatlimab)과 옵디보(Opdivo) 병용요법의 임상 2/3상에서 LAG-3 억제제의 통계적 유의성을 확인한 바 있다.
LAG-3 억제 기능을 탑재한 ABL501 역시 LAG-3 단독요법, PD-L1 단독요법, 그리고 LAG-3와 PD-L1 병용요법 대비 개선된 항암효과를 입증하면서 기존 PD-(L)1 기반 치료제의 한계를 극복할 수 있는 새로운 치료 대안으로 주목받고 있다.
앞서 에이비엘바이오는 지난 11월 9일 항암신약 후보물질 ‘ABL103’ 개발 프로젝트가 정부의 국가신약개발사업 과제로 선정됐다고 밝힌 바 있다.
현재 비임상 단계인 ABL103은 B7-H4와 4-1BB를 동시에 표적하는 유방암 및 난소암 치료 이중항체 면역항암제로, first-in-class 개발이 가능하다. B7-H4는 기존 면역항암제의 효과가 상대적으로 미미한 암종에서 단독 또는 병용 투여를 통해 다양한 치료 가능성을 열어줄 것으로 회사 측은 보고 있다.
에이비엘바이오 관계자는 “올해 ABL103에 이어 ABL501이 국가신약개발사업 과제로 연이어 선정됐다. 특히 ABL501은 지난해 4월 한국보건산업진흥원의 국책과제 선정에 더해 또다시 정부 지원 대상으로 선정될 만큼 신규 치료제로서의 개발 가능성이 뛰어난 후보물질”이라며, “이번 과제를 통해 ABL501의 임상 1상을 성공적으로 마무리하고, 임상 2상 승인을 위한 기틀을 마련하겠다”고 말했다.
[바이오타임즈=김수진 기자] sjkimcap@biotimes.co.kr


