암세포를 선택적으로 치료하는 항체와 TPD의 촉매 메커니즘을 결합
이중 정밀 표적 단백질 분해 접근법의 기술 잠재력 입증

[바이오타임즈] 차세대 항체 플랫폼 기반 혁신 신약 개발 기업 오름테라퓨틱(대표 이승주)이 6일 항암제 분야의 글로벌 리더인 브리스톨-마이어스 스퀴브(Bristol Myers Squibb, BMS)와 총 2,334억 원 규모의 기술이전 계약을 체결했다고 밝혔다.
이번에 기술이전에 성공한 후보물질 ORM-6151은 최초(first-in-class)의 항 CD33 항체 기반 GSPT1 단백질 분해제 약물로, 급성 골수성 백혈병(AML) 또는 고위험 골수형성이상증후군 환자 치료를 위한 FDA 임상 1상 시험계획을 승인받은 바 있다.
BMS는 이번 인수 거래에 따라 오름테라퓨틱에 계약금 1억 달러(약 1297억 원)를 지불하고, ORM-6151 프로그램을 확보했다. 이후 추가 마일스톤을 포함해, 오름테라퓨틱은 총 1억 8,000만 달러(약 2334억 원)를 확보하게 된다. 그 외 자세한 내용은 공개되지 않았다.
이번 계약은 페렐라 와인버그 파트너스(Perella Weinberg Partners)가 재무 자문을, 스턴 케슬러 골드스타인 앤 폭스(Sterne Kessler Goldstein & Fox)와 스캐든, 아프스, 슬레이트, 미거 앤 플롬(Skadden, Arps, Slate, Meagher & Flom LLP)이 법률 자문을 맡았다.
오름테라퓨틱은 자체 개발한 TPD²(Dual-precision Targeted Protein Degradation) 기술 및 TPS²(Dual-precision Targeted Protein Stabilization) 기술을 보유하고 있다.
TPD²는 오름테라퓨틱이 세계 최초로 TPD를 ADC 형태로 항체에 결합한 기술이다. 쉽게 말해 항체 약물 접합체(ADC)에 표적 단백질 분해제(TPD)를 융합하는 기술이다. 항체와 결합된 페이로드는 암세포에 특이적으로 전달돼, 세포 내 표적 단백질 GSPT1을 분해하고, 종양 세포 사멸을 유발하도록 설계했다.
표적 단백질 분해기술(Target Protein Degradation, TPD)은 체내 단백질 분해 시스템을 모방한 화합물을 이용해 질병 단백질을 분해·제거하는 기술이다. 전통적인 방식으로 치료가 어려웠던 질병 단백질을 원천적으로 제거하거나 기존 약물에 대한 내성을 극복할 수 있는 새로운 치료법으로 주목받고 있으며, 프로탁 기술, 분자 접착제 기술 등이 있다.
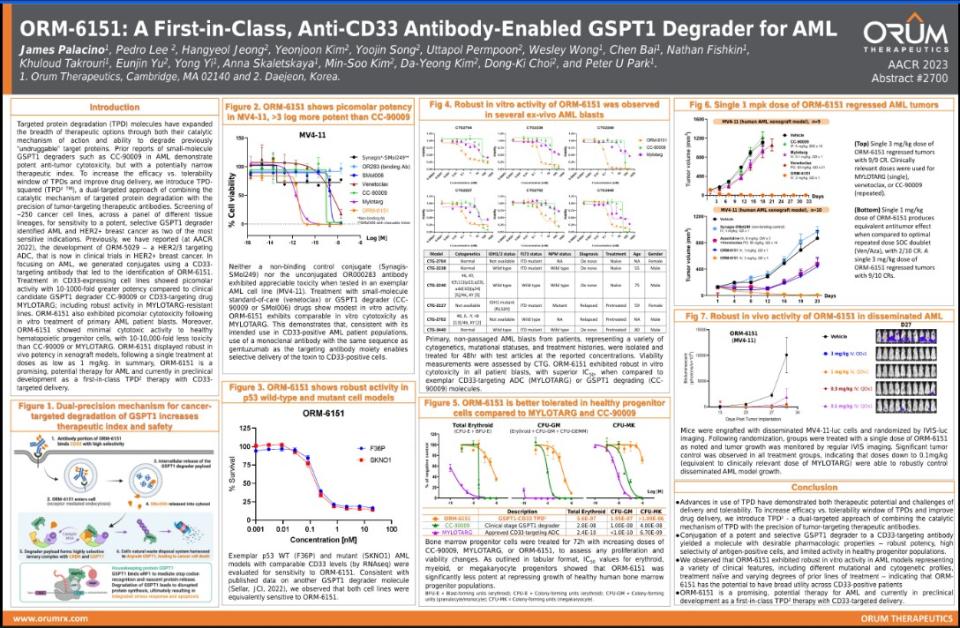
◇이중 정밀 표적 단백질 분해 접근법의 기술 잠재력 입증
회사는 TPD² 기술을 기반으로 ORM-5029와 ORM-6151을 선보였고, 각각 유방암과 급성골수성백혈병(Acute Myeloid Leukemia, 이하 AML) 치료를 목적으로 한다.
ORM-6151은 오름테라퓨틱의 TPD² 플랫폼을 활용한 두 번째 후보물질로, 암세포 표면에 과발현된 ‘CD33’을 표적하는 항체와 ‘GSPT1’ 분해제를 결합한 것이다. 즉, 암세포를 선택적으로 치료하는 항체와 TPD의 촉매 메커니즘을 결합한 원리다.
ORM-6151은 전임상에서 다양한 돌연변이와 치료 이력을 가진 여섯 개 환자 유래 세포주에서 기승인된 ADC 치료제인 ‘마일로타그(Mylotarg)’와 BMS사가 임상을 진행 중인 GSPT1 분해제 ‘CC-90009’ 대비 10~1,000배 더 강력한 효능을 보였다. 또한, 정상 골수 조혈모세포에서는 두 약물 대비 ORM-6151의 효능이 낮음을 보임으로써 보다 월등한 내약성을 확인했다.
ORM-6151은 P53 유전자 돌연변이 세포주에서도 wild type 세포주와 동등한 효능을 보였다. 이는 기존 치료제인 베네토클락스(Venetoclax)와 아자시티딘(Azacitidine)에는 낮은 반응률을 보이는 P53 돌연변이에 대한 미충족 수요를 채울 수 있다는 가능성을 시사한다.
이외에 현재 미국 임상 1상을 진행 중인 ORM-5029는 오름의 첫 번째 플랫폼 기술인 TPD²(Dual-Precision Targeted Protein Degradation)를 활용한 것으로, 일반 세포가 아닌 특정 표적세포 내의 GSPT1 만을 효과적으로 분해하는데 특화했다. 임상적으로 검증된 항체인 ‘퍼투주맙’에 GSPT1 분해제를 결합한 HER2 표적 ADC다. 이는 단백질 분해의 효능 대비 내약성 기간을 늘리고, 약물 전달을 개선한 것이다.
회사는 최근 ASCO에서 ‘HER2 발현 진행성 고형 종양 환자를 대상으로 HER2 표적 GSPT1 분해제인 ORM-5029에 대한 최초의 임상 1상 시험’의 디자인을 공개한 바 있다. 더불어, 세계 최초로 단백질 분해에 중심 역할을 하는 ‘E3 리가아제’를 저해하는 물질을 ADC 형태로 항체에 결합한 TPS²(Dual-precision Targeted Protein Stabilization) 기술을 통해 면역항암제 개발을 추진 중이다.
오름테라퓨틱의 또 다른 기술인 TPS²는 세계 최초로 단백질 분해에 핵심 역할을 하는 E3 리가아제(ligase)를 저해하는 물질을 항체에 결합한 ADC 기술이다. 즉, 단백질 저해제와 항체를 결합한 기술로, 지난 4월 미국암연구학회(AACR)에서 처음 선보였다.
이승주 오름테라퓨틱 대표는 “BMS는 단백질 분해 분야에서 오랜 전통을 가진 항암제 분야의 글로벌 리더이며, 이번 계약을 통해 오름이 자체 개발한 ‘이중 정밀 표적 단백질 분해 접근법(TPD², Dual-Precision Targeted Protein Degradation)’의 기술 잠재력이 입증된 것”이라고 말했다.
또한 “오름은 표적 단백질 분해제의 약물의 치료 범위(therapeutic window)를 넓히고, 표적 단백질 분해제의 잠재력을 최대화하기 위해 ADC의 형태로 암세포에 특이적으로 전달하는 접근방법을 선도하고 있다”고 덧붙였다. 그는 “BMS가 암 환자에게 임팩트 있는 치료제로 개발될 수 있는 ORM-6151 프로그램을 이전받아가게 되어 매우 기대된다”고 덧붙였다.
한편 오름테라퓨틱은 2016년 설립해, 자체 개발한 TPD²(티피디 스퀘어) 접근방법을 적용한 차세대 TPD 플랫폼들을 개발 중이다. 항체와 단백질 분해제를 결합해 기존에 접근할 수 없었던 다양한 항암제를 준비하고 있다. 본사는 대전에 위치하며, 대전과 미국 보스턴에 연구소를 운영하고 있다. 브릿지 라운드까지 총 1,260억 원 규모의 투자를 유치했다.
이승주 오름테라퓨틱 대표는 미국 UC버클리에서 박사학위를 받은 후 2년간 스탠퍼드대에서 박사후연구원을 거친 뒤 LG생명과학(現 LG화학)에서 연구 내공을 쌓았다. 그는 입사 5년 만에 글로벌 제약기업 사노피로 자리를 옮겨 아시아연구소장까지 역임했다. 이 대표는 글로벌 신약 개발 경험을 계기로 김용성 아주대 공대 교수와 오름테라퓨틱을 공동 창업했고, 초기부터 글로벌 시장 진출 전략을 전개했다.
[바이오타임즈=김수진 기자] sjkimcap@biotimes.co.kr


