최초 치료로 마약류 진통제 사용 금지하고, 가급적 항불안제 1개 품목 처방
[바이오타임즈] 최근 10대 청소년들이 마약류 진통제 ‘펜타닐 패치’를 투약·유통하는 사건이 적발되면서 마약 오남용에 대한 우려의 목소리가 높아지고 있다.
또한 정부가 하수 속에 녹아있는 성분을 바탕으로 국내 마약 사용 실태를 유추하는 사업을 벌인 가운데, 전국 57개 하수처리장에서 필로폰 등 마약과 관련한 성분이 검출되는 등 마약 청정국이라 불리던 우리나라는 이미 전국적으로 마약이 유통돼 사용되고 있는 것으로 드러났다.
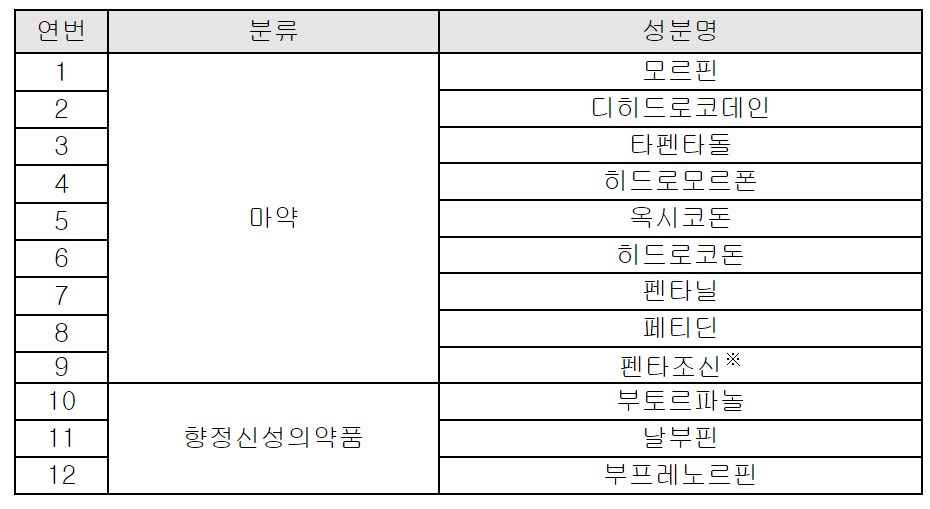
이에 식품의약품안전처는 오남용의 가능성이 크고 의존성을 일으키기 쉬운 의료용 마약류 진통제 12종과 항불안제 10종의 적정한 처방과 투약 등을 위한 안전 사용 기준을 마련하여 일선 의료현장에 배포한다고 밝혔다.
◇ 최초 치료로 비약물적 치료나 비 마약류 진통제 치료 우선 권고
식약처는 우선 의료용 마약류 진통제는 오남용 가능성이 큰 약물이므로 주의하여 사용해야 하며, 최초 치료로 사용하지 않아야 한다고 권고했다. 비약물적 치료 또는 비 마약류 진통제(아세트아미노펜, 이부프로펜 등)의 약물치료를 우선으로 해야 한다는 것이다.
마약류 진통제는 만 18세 이상의 환자에게 처방하되 효과가 있는 가장 낮은 용량을 사용하고, 최초 처방 시에는 1회 처방 시 7일 이내로 단기 처방하며, 추가 처방 시에도 가능한 1개월 이내로, 최대 3개월 이내로 처방해야 한다.
특히 최근 10대 청소년 오남용 및 불법유통 사례가 적발됨에 따라 펜타닐 패치의 허가사항 및 동 안전기준에 따라 18세 미만의 비암성 통증에 처방하지 않도록 일선 의료현장에 협조를 재요청했다.
의료용 마약류 진통제인 펜타닐 패치제는 마약류 진통제의 투여 경험이 없는 환자에게 최초로 사용하지 않아야 하며, 허가사항의 투여 간격을 준수할 것을 권장했다.
아울러 안전성 확보 및 오남용 방지를 위한 추가방안으로 △‘의료용 마약류 빅데이터 활용 서비스’를 통한 환자의 의료용 마약류 투약 이력을 확인하고 △마약류 진통제 사용 시 의존성, 중독증상, 금단증상 및 호흡 억제 증상 등 환자의 상태를 신중히 관찰할 것을 제시했다.
◇ 의료용 마약류 항불안제는 가급적 1개 품목만 처방해야
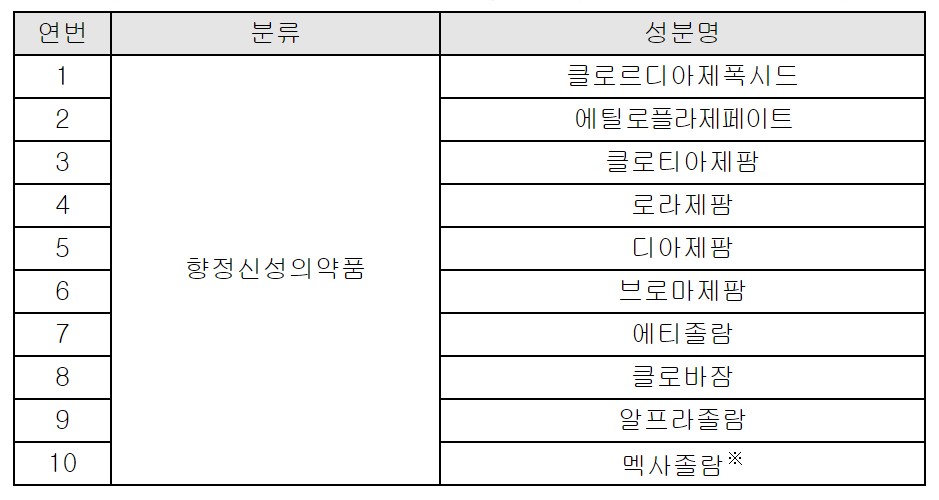
한편 식약처는 의료용 마약류 항불안제 처방·사용 원칙에 대한 기준도 마련했다.
항불안제는 의존성을 일으킬 수 있음을 항상 인식하여 1개 품목을 허가된 용량 내에서 최소 유효 용량으로 사용하는 것을 원칙으로 하되, 가능한 1회 처방 시 30일 이내로 처방하고, 소아와 고령자는 저용량부터 시작하여 주의 깊은 관찰 하에 신중히 투여할 것을 권장했다.
특히 벤조디아제핀계 약물의 병용투여는 약물의존성 및 중추신경계 억제의 위험성을 증가시킬 수 있어 1개 품목을 허가사항 범위 내에서 처방하는 것을 원칙으로 해야 한다.
현재 진통제 시장은 마약성 진통제 오피오이드계(아편) 약물이 절반 이상을 차지하고 있다. 오피오이드는 마약성 진통제로 급성 통증이나 암과 관련된 통증을 완화하는 데 사용된다. 약물 의존성 및 복용량 증가, 호흡 곤란, 사망 위험이 있지만 지난 10년간 사용량이 점차 늘었다.
우리나라는 OECD 국가 중 상대적으로 오피오이드 처방률이 낮은 편이지만, 전체 마약성 진통제 이용 빈도가 낮은 것은 아니다. 식약처가 발표한 2019년 우리나라 의료용 마약류 사용 현황 분석 결과에 따르면 전체 국민 중 353만 명에 해당하는 환자가 마약성 진통제를 처방받았다. 이는 국민 약 14.7명 가운데 1명이 마약성 진통제를 이용한 셈이다.
최근 전 세계적으로 마약성 진통제의 사용 증가와 부작용 등이 속출하면서 비마약성 진통제 혁신 신약 개발에 대한 요구도 높아지고 있으며, 국내 바이오·제약기업들의 개발 경쟁도 뜨겁다.
식약처는 앞으로 ‘사전알리미’, ‘자발적 보고’ 제도 등을 통하여 의료용 마약류 진통제와 항불안제의 오남용을 관리해 나가고, 경찰청·심평원 등 유관 기관과 기획 합동 감시를 실시해 국민이 안전하게 의료용 마약류를 사용할 수 있는 환경이 조성될 수 있도록 노력하겠다고 밝혔다.
[바이오타임즈=박세아 기자] news@biotimes.co.kr


