CP-COV03, 니클로사마이드를 주성분으로 개발한 범용 항바이러스제
20세기 대표적 범용 항생제인 페니실린처럼 혁신적인 항바이러스제 탄생 기대
[바이오타임즈] 현대바이오가 세계적 유행 조짐을 보이는 원숭이두창(Monkeypox, 원두) 사태를 해결하기 위해 자사의 범용 항바이러스제 후보 약물에 관해 미국 식품의약국(FDA)에 패스트트랙(Fast Track)을 신청하기로 결정했다.
현대바이오는 신종 코로나바이러스 감염증(코로나19) 치료를 위해 먹는 항바이러스제로 개발한 CP-COV03을 원숭이두창 치료제로 사용할 수 있도록 할 예정이다.
회사의 이 같은 결정은 미국 현지의 바이오 분야 전문 로펌을 통해 CP-COV03가 ‘동물실험갈음규정’(Animal Rule) 적용으로 패스트트랙이 가능하다는 사실을 확인하고 결정한 것으로 알려졌다.
동물실험갈음규정은 미국 등 주요국이 천연두나 원두처럼 사람을 대상으로 한 임상시험이 불가능하거나 비윤리적일 경우 동물실험 결과만으로 치료제로 승인하는 제도로, 일종의 패스트트랙 절차다. FDA는 2018년 미 제약기업인 시가 테크놀로지가 동물실험을 거쳐 천연두 치료용으로 개발한 ‘티폭스’(TPOXX)를 천연두 치료제로 승인한 것을 비롯해 지금까지 13종의 약물에 애니멀 룰을 적용해 신약으로 승인한 바 있다.
회사 측은 FDA에 CP-COV03의 그간 동물실험 결과 등 관련 자료도 신속히 제출하기로 했다.
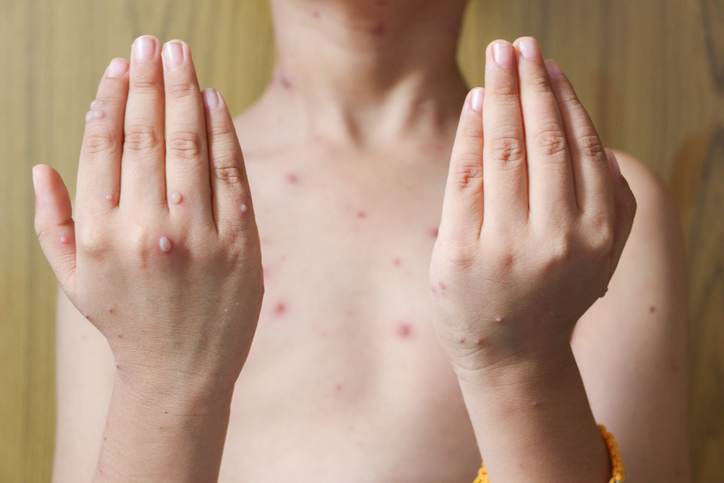
그간 아프리카 풍토병으로 알려진 원숭이두창은 올해 5월부터 미국과 유럽 등의 18개국에서 100여 건의 감염과 의심 사례가 보고되고 있다. 사람 간에는 병변과 체액, 호흡기 비말, 침구 등 오염된 물질과의 접촉을 통해 감염되고, 두통과 38.5도 이상 고열, 림프 부종과 근육통, 피부 병변 등이 나타난다.
세계보건기구(WHO)에 따르면 원숭이두창은 40년간 존재했던 질병으로, RNA 바이러스에 비해 변이 가능성이 훨씬 낮고, 천연두 백신이 효과가 있어 크게 우려할 수준은 아니라고 밝혔다.
그러나 최근 이례적으로 풍토병이 아닌 국가에서 원숭이두창이 발생하고 있어, 국내 유입 가능성도 점차 커지고 있다.

◇CP-COV03, 니클로사마이드를 주성분으로 개발한 범용 항바이러스제
현대바이오가 개발 중인 항바이러스제 CP-COV03의 주성분인 니클로사마이드는 원두 바이러스에 효능이 탁월하다는 학계의 실험 결과도 이미 나와 있다.
미 캔자스대 연구진은 니클로사마이드가 1마이크로몰의 낮은 농도에서도 원두 바이러스와 같은 계열인 백시니아 바이러스 증식을 무려 100분의 1 수준으로 낮추는 효능을 발휘한 세포실험 결과를 2020년 7월 국제학술지인 ‘백신즈’(Vaccines)를 통해 공개한 바 있다. 연구진은 총 3,228종의 현존 약물을 대상으로 약효 표적을 세포로 하고, 내성을 일으키지 않으면서 효능을 발휘하는 약물을 찾기 위한 실험을 진행한 끝에 4종의 후보를 찾았는데 이 중 FDA 승인을 받은 것은 니클로사마이드가 유일했다.
현대바이오는 사스, 메르스, 에볼라, 지카 등 팬데믹급 바이러스 사태 때마다 최고의 치료제 후보로 꼽혔지만, 과학자들이 수십 년간 해결하지 못한 니클로사마이드의 생체이용률 난제를 첨단 DDS 기술 등을 통해 해결하는 데 세계 최초로 성공, CP-COV03을 개발했다.
FDA가 애니멀 룰을 적용할 경우, 그간 동물실험에서 약물의 안전성이 검증된 CP-COV03은 현재 진행 중인 코로나19 임상2상에서 혈중 유효 약물 농도(PK)와 안전성이 확인되면 원두에 감염된 동물 효력실험을 통해 원두 치료제로 곧바로 승인받을 수 있다.
이에 따라 현대바이오는 CP-COV03의 코로나19 임상2상의 신속한 진행을 위해 다음 주부터 임상 수행병원을 확대하는 등 임상 진행 속도 제고에 박차를 가하기로 했다.
CP-COV03는 약효가 세포를 표적하는 니클로사마이드 기반으로, 바이러스가 침입하면 세포가 그 바이러스를 이물질로 인식, 제거하도록 하는 세포의 오토파지(Autophagy, 자가포식) 작용을 촉진하는 범용 항바이러스제 후보물질이다. 약리작용 메커니즘이 모든 바이러스에 적용 가능하다는 과학계의 평가를 받아왔다.
현대바이오 오상기 대표는 “CP-COV03는 모든 바이러스 제거가 가능한 메커니즘의 니클로사마이드를 주성분으로 개발한 범용 항바이러스제”라며 “FDA의 패스트트랙으로 CP-COV03가 원두 치료제가 되면 20세기 대표적 범용 항생제인 페니실린처럼 혁신적인 항바이러스제가 탄생하는 것”이라고 의미를 부여했다.
한편 중앙방역대책본부는 두창 백신과 관련해 “생물 테러 등 고도의 공중보건위기에 대응해서 사용할 목적으로 생산해서 비축하고 있다. 원숭이두창이 있다고 하더라도 일반 인구에 대한 당장의 사용 계획은 검토되고 있지 않다”고 밝혔다. 방역 당국에 따르면 국내 두창 백신 보유량은 3,502만 명분이다.
[바이오타임즈=김수진 기자] sjkimcap@biotimes.co.kr


