표적 물질 응집 억제 성공…치매 신규치료제 개발 단초 제공
후속 연구 통해 저해제의 효과를 표적 영역으로 집중시킬 계획

[바이오타임즈] 치매는 노인에게 기억력 및 다른 지적 능력의 감퇴가 오는 것을 말한다. 과거 치매는 대개 정상적인 노화 과정에서 오는 증상으로 여겨졌지만, 현대사회에서는 다양한 원인에 의해 발생되는 특별한 질병의 개념으로 받아들여지고 있다.
세계보건기구(WHO)에 따르면 2025년 전 세계 치매 환자 수는 1억 4,000만 명으로 전망된다.
치매는 다양한 원인에 의해 발생하며 그 원인에 따라 구분하는데, 약 62% 이상이 알츠하이머성 치매다. 우리나라 역시 65세 이상 치매 환자 4명 중 3명은 알츠하이머형 치매이다.
알츠하이머병(Alzheimer's disease)은 치매의 가장 흔한 유형으로 처음 보고된 지 약 100년이 지났지만, 아직도 정확한 발병기전이 밝혀지지 않았다. 다만, 아밀로이드 베타(Aβ)로 구성된 병원성 아밀로이드 섬유 응집체에 의한 연쇄적인 작용으로 발병된다는 아밀로이드 가설이 가장 유력하다고 알려졌다. 비정상적으로 39~43개의 아미노산으로 잘린 아밀로이드 조각들의 응집체가 뇌에 쌓이면서 시냅스 손상과 세포 독성으로 발병한다는 것이다.
알츠하이머병을 치료하기 위해 세계적으로 아밀로이드 베타 단백질의 섬유 응집체를 표적으로 하는 항체 치료제 연구가 활발히 진행되고 있다.
최근 아두카누맙(Aducanumab)과 레카네맙(Lecanemab)은 알츠하이머병에 대한 약물 사용 승인 허가를 받으면서 대증요법(Symptomatic Therapy)이 아닌 근본적인 치료제로써는 최초로 치매 치료제 사용 승인을 받으며 주목받고 있다.
그러나, 아두카누맙은 Aβ를 감소시켰지만 임상시험에서 효능이 없는 것으로 나타나면서 Aβ 단백질 가설 자체에 대한 신뢰를 떨어뜨리기도 했다. 또한, 여전히 많은 치매 치료제 후보물질이 증상 완화 효과가 부족해 약물로 승인받지 못한 상황이다.
따라서, 치매 치료제의 다양화와 효율 증대를 위해서는 아밀로이드 베타 단백질 응집의 분자적 기전을 이해하고 이를 제어하기 위한 기술 연구가 필요한 가운데, 국내 연구진이 알츠하이머병을 유발하는 병원성 아밀로이드 응집체의 형성과정을 규명하여 신규 치료제 발굴의 실마리를 제공했다.
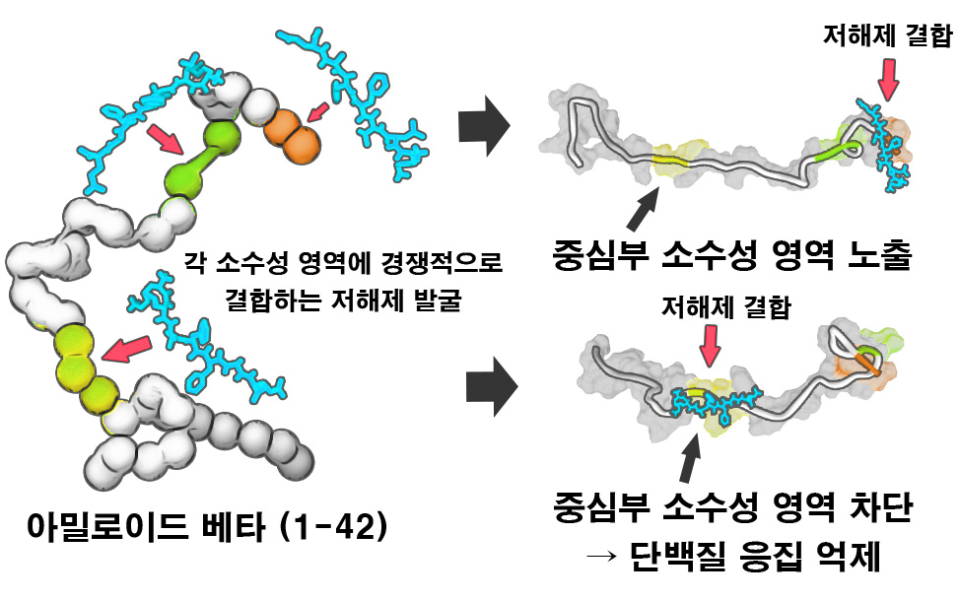
◇알츠하이머병 유발하는 아밀로이드 베타의 응집 과정, 분자 수준에서 규명
한국연구재단은 김준곤 교수(고려대학교)와 최정모 교수(부산대학교) 연구팀이 알츠하이머병을 유발하는 것으로 알려진 단백질인 아밀로이드 베타의 응집 과정을 규명하고, 이를 기반으로 단백질의 병원성 아밀로이드 응집체 형성을 억제하는 신규 응집 억제제를 발굴했다고 밝혔다.
과학기술정보통신부와 한국연구재단이 추진하는 기초연구사업의 지원으로 수행된 이번 연구의 성과는 화학 분야 국제학술지 ‘미국화학회 골드지(JACS Au)’에 3월 2일 게재됐다.
알츠하이머병 환자의 뇌 부검 시 발견되는 아밀로이드 플라크(Amyloid Plaques)는 주요 병리학적 징후로 알려져 있으며, 이를 제거함으로써 알츠하이머병을 치료하고자 천연물, 소립자 수용체, 항체 등 다양한 형태로 치료제 후보물질이 개발됐다.
치매 치료제의 다양화와 효율 증대를 위해서는 아밀로이드 베타 단백질 응집의 분자적 기전을 이해하고 이를 제어하기 위한 기술 연구가 필요하다.
아밀로이드 베타 단백질은 본래 어떤 특정한 구조를 이루고 있지 않은 비정형 단백질이다. 이에 연구팀은 구조가 없는 단백질의 특성을 분석하고 구조가 없는 와중에 일시적으로 형성되는 분자 내부 및 분자 간 상호작용을 관찰하기 위해 다양한 실험 장비를 종합적으로 활용했다.
예를 들면 포항 가속기연구소의 지원으로 용액상에서 존재하는 비정형 단백질의 다양한 구조적 특성을 관찰할 수 있었고, 고려대학교 유전 단백체 연구센터의 질량분석기를 활용해 다양한 환경에서 단백질을 관찰해 가속기연구소에서 수행한 실험 결과와 교차검증했다. 또한 실제 실험으로 관찰하기 어려운 부분은 국가 슈퍼컴퓨팅센터의 지원으로 대규모의 구조 전산 모사 실험을 수행해 완성도 높은 연구성과를 확보할 수 있었다는 설명이다.
이를 통해 연구팀은 아밀로이드 베타 단백질의 각 영역이 병원성 아밀로이드 응집체 형성과정에 참여하는 역할을 규명해, 아밀로이드 베타 단백질 응집을 억제하기 위한 핵심 표적 영역을 특정했다.
아밀로이드 베타(1-42) 단백질의 응집 현상은 중심부 소수성 영역이 외부로 노출되어 있어야 발생한다는 것을 규명했다.
즉, 아밀로이드 베타 (1-42) 단백질은 크게 3가지 소수성 영역(17번 류신부터 19번 페닐알라닌까지; 32번 아이소류신부터 34번 류신까지; 41번 아이소류신과 42번 알라닌)으로 구성되어 있으며, 그중에서 단백질 응집 과정에서 중요한 역할을 하는 병인 단백질의 소수성 영역을 규명하기 위해 용액상 X선 소각산란 실험을 수행했고, 단백질의 C 말단부 소수성 영역(32번 아이소류신부터 34번 류신까지)이 중심부 소수성 영역(17번 류신부터 19번 페닐알라닌까지) 혹은 C 말단부(41번 아이소류신과 42번 알라닌)와 일시적인 상호작용을 이루는 것을 확인했다.
또한, 인공지능 기반 단백질 복합체 구조예측을 통해 단백질의 각 소수성 영역에 결합하는 저해제 후보물질을 발굴했으며, 실험을 통해 단백질 응집 저해 및 신경 세포 독성 완화 효과를 확인했다.

◇후속 연구 통해 저해제의 효과를 표적 영역으로 집중시킬 계획
고려대학교 김준곤 교수는 “아밀로이드 베타 단백질이 응집되는 과정을 분자 수준에서 규명하여 응집 과정을 억제할 수 있도록 발표한 것이므로 본 연구 결과를 바탕으로 다양한 신규 단백질 응집 저해제가 발굴될 것으로 기대하고 있다”고 말하며 “최근 발전한 데이터베이스 기반 인공지능 단백질 구조예측 기술을 대규모의 구조 전산 모사 실험과 접목해 비정형 단백질을 대상으로 활용했다는 점과 비정형 단백질 간의 일시적인 상호작용을 다양한 실험 기법을 활용해서 규명했다는 점은 이 연구 방법론을 확장 적용하면 다른 퇴행성 신경질환의 치료제 개발에도 응용할 수 있음을 의미한다”고 설명했다.
연구팀은 아밀로이드 베타 단백질 응집의 핵심 영역을 비활성화하는 방식으로 다양한 유형의 신규 응집 저해제를 발굴하면 치매 치료제 후보물질로 활용 가능할 것으로 기대하며, 후속 연구를 통해 저해제의 효과를 표적 영역으로 집중시킬 계획이다.
[바이오타임즈=김수진 기자] sjkimcap@biotimes.co.kr


