37℃에서 30분의 반응을 통해 다량의 RNA 증폭 산물을 생성하는 효율적인 유전자 증폭법
저렴하고 소형화 현장 시스템의 구현이 용이한 기술
바이러스, 박테리아 및 암에 신속하게 대응할 수 있는 원천기술로도 활용될 수 있을 것

[바이오타임즈] 최근 코로나바이러스가 점차 엔데믹 양상을 보이고 있지만, 많은 전문가는 오미크론과 같은 변이 바이러스가 언제든지 출현해 유행할 가능성이 크다고 말한다.
코로나19 종식을 위해서는 미래에 나타날 신종 바이러스까지 신속하고 정확하게 검출할 수 있는 분자진단 기술의 필요성이 대두되는 가운데, 국내 연구진이 코로나19는 물론 변이 바이러스까지 한 번에 검출할 수 있는 분자진단 기술을 개발했다.
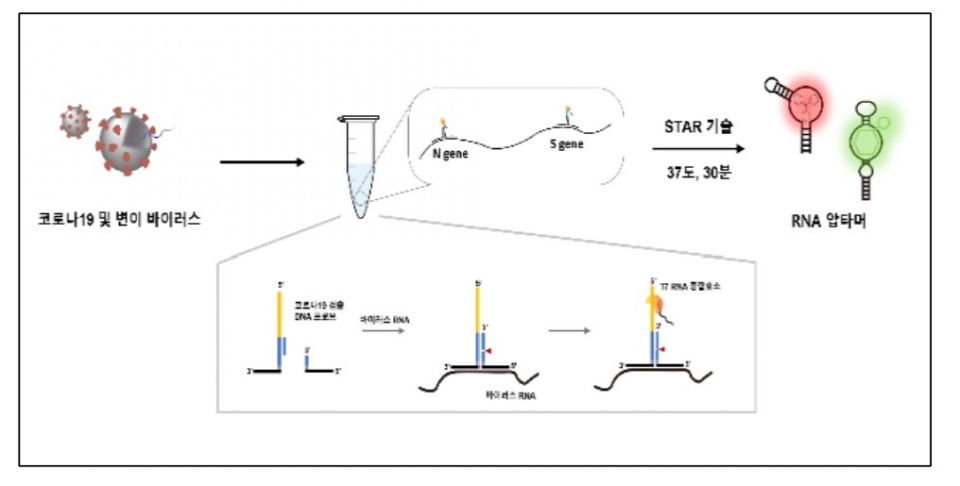
◇건국대 박기수 교수연구팀, 등온 핵산 증폭 기술 활용 분자진단 기술 개발
한국연구재단은 건국대학교 박기수 교수연구팀이 등온 핵산 증폭 기술을 활용해 코로나19 및 변이 바이러스를 한 번에 검출할 수 있는 분자진단 기술을 개발했다고 밝혔다.
과학기술정보통신부와 한국연구재단이 추진하는 우수신진연구사업의 지원으로 수행된 이번 연구의 성과는 바이오센서 분야 국제학술지 ‘바이오센서스 앤드 바이오일렉트로닉스(Biosensors and Bioelectronics)’에 3월 31일 온라인 게재됐다.
지금까지 코로나19 진단은 사스코로나바이러스-2(SARS-CoV-2)의 핵산을 유전자 증폭 기술로 확인하는 분자진단과 항원·항체 반응에 기반하는 면역진단으로 진행됐다.
면역진단은 검체 내에 포함된 항원 바이러스를 직접 검출하는 항원 진단(Viral Antigenic Test)과 감염된 사람의 혈청에 존재하는 항체를 검출하는 혈청 면역검사(Serological Test)로 구분할 수 있다. 이러한 면역 검사법은 매우 간편하고 신속하며, 비용이 비교적 저렴하지만, 핵산을 검출하는 분자진단에 비해서 진단의 정확도가 낮다.
또한, 감염된 사람의 혈청에서 IgM과 IgG 항체의 유무를 검출하는 혈청 면역검사의 경우, 감염 초기에는 (1~3일) 정확한 진단이 불가능하다는 단점이 있다. 이러한 문제점 때문에 우리나라를 비롯한 많은 나라에서 코로나19 진단의 표준방법으로 핵산 증폭[RT-PCR(Reverse Transcription-PCR)]을 통한 분자진단을 널리 채택하고 시행하고 있다.
현재 코로나19 검출을 위한 표준 분자진단 방법으로 쓰이는 PCR(Polymerase Chain Reaction, 중합효소 연쇄반응)은 온도조절 과정에 기반한 표적 핵산 증폭 기술이다. PCR은 인간의 DNA를 증폭하여 여러 종류의 유전질환을 진단하는 데도 사용된다.
PCR은 현재 유전물질을 조작하여 실험하는 거의 모든 과정에 사용하고 있는 검사법으로, 세균이나 바이러스, 진균의 DNA에 적용해 감염성 질환의 진단 등에 사용할 수 있다. 그러나, 이 검사 방법은 유전자를 증폭하는 과정에서 상당한 시간이 소요된다. 또한, 정교한 온도조절을 위한 고가의 분석 장치 및 숙련된 기술이 필요하여 현장에서 신속하게 수행할 수 없다는 단점이 있다.
◇37℃에서 30분의 반응을 통해 다량의 RNA 증폭 산물을 생성하는 효율적인 유전자 증폭법
건국대 박기수 교수연구팀이 개발한 ‘신규 등온 핵산 증폭 기술(STAR, split T7 promoter-based isothermal transcription amplification with light-up RNA aptamer)’은 변이 바이러스를 포함한 코로나 바이러스, 박테리아 등을 37℃에서 30분 만에 신속 진단할 수 있다. 등온 핵산 증폭 기술이란 반복적인 온도조절 과정 없이 등온에서 표적 핵산을 증폭하는 기술을 말한다.
STAR는 바이러스의 유무뿐만 아니라 종류 구분도 가능하며, 기존 PCR 및 등온 핵산 증폭 기술 기반 분자진단 방법과 달리, 반응 개시 전 온도조절 과정이 필요 없고 하나의 효소(T7 RNA 중합효소)만을 이용, 37℃의 일정한 온도에서 반응이 진행된다.
RNA를 검출할 시 대부분의 핵산 증폭 기술은 cDNA로의 전환이 필요하며 이 과정에서 효소 한 개가 추가로 사용되는데, 연구팀은 이를 보완하고자 RNA를 직접 검출할 수 있는 Three-way Junction(3-방향 접합) 구조를 도입하여 추가적인 효소의 첨가 없이 RNA의 직접적인 검출을 진행했다.
특히, 기존 PCR 기술의 경우, RNA를 cDNA로 전환하는 과정 후에 증폭이 진행되기 때문에 DNA에 의한 교차오염 가능성이 크며, 이로 인한 위양성(False Positive) 가능성이 높았다. 하지만, 이번 기술은 RNA를 바로 인식하여 증폭이 이루어지기 때문에 기존의 문제점을 극복할 수 있으며, 정확한 분석이 가능하다.
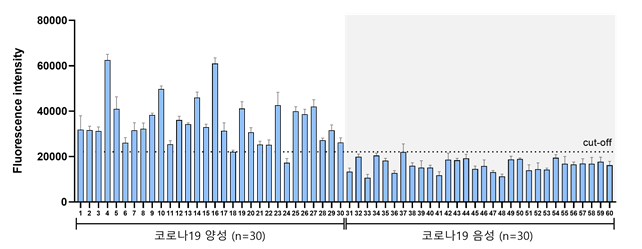
연구팀은 STAR을 전남대학교병원 최현정 교수 연구팀을 통해 확보된 60여 명의 실제 임상 샘플에 적용한 결과, 코로나19에 대해 높은 민감도(96.7%)와 특이도(100%)를 보임을 확인했으며, 바이러스, 박테리아 및 암 등 다양한 핵산 바이오 마커 검출 시 활용 가능할 것으로 내다봤다.

◇저렴하고 소형화 현장 시스템의 구현이 용이한 기술
연구팀은 PCR로 대표되는 현재의 유전자 분석 기술을 대체할 수 있는 대안 기술로의 활용 가능성이 크다고 판단하며, 다양한 질병으로 확장 가능성을 검증하고, 대량 생산을 위한 분자진단키트 제작이 진행될 필요가 있다고 생각한다.
다만, 현장에서 손쉽게 결과를 확인할 수 있는 시스템 구현을 위해 추가연구가 필요하며, 기술의 확장성 검증을 위해 다양한 핵산 바이오 마커 검출 연구가 지속해서 이루어져야 한다는 설명이다.
박기수 교수는 “본 연구팀이 개발한 기술은 37℃에서 30분의 반응을 통해 다량의 RNA 증폭 산물을 생성하는 효율적인 유전자 증폭법으로서, 코로나19 및 관련 변이 바이러스를 한 번에 검출해낼 수 있으며, 저렴하고 소형화 현장 시스템의 구현이 용이한 기술”이라고 설명했다.
이어 박 교수는 “2023년에는 글로벌 분자진단시장이 약 220.3억 달러 규모에 이를 것으로 전망되는 상황에서 국내의 독자적인 기술로 개발된 제품으로 막대한 경제적 파급효과를 가져올 수 있으며, 국제적 경쟁력을 크게 높일 수 있다”라며 “핵심 기술을 바탕으로 코로나 19 바이러스뿐만 아니라 미래에 나타날 새로운 바이러스, 박테리아 및 암에 신속하게 대응할 수 있는 원천기술로도 활용될 수 있을 것”이라고 덧붙였다.
[바이오타임즈=정민구 기자] news@biotimes.co.kr


