탈모치료제, LNP 기반 대장암·췌장암 치료제 임상시험 진행 목표
[바이오타임즈] 나노-의약 기술 전문기업 ㈜무진메디(대표이사 윤태종, 322970)가 무균 약물 제제 GMP 생산시설 시스템을 구축하고 사업별 파이프라인 확보를 가속한다.
㈜무진메디는 지난 9월 경기도 하남시 풍산동 ‘유테크밸리’ 10층(720평 규모)으로 본사를 이전하고 내년 7월 완공을 목표로 의약품 제조 및 품질관리 기준(GMP)에 맞춘 생산시설 구축에 착수했다. 회사는 무균 의약품 제제 등급의 나노입자(Nanopaticle) 전용 GMP 시설 구축을 통해 도포형 탈모 치료제와 나노 입자 전달체(lipid nanoparticle, LNP) 기반의 대장암, 췌장암 치료제 임상시험을 진행할 계획이다.
2016년 설립된 ㈜무진메디는 인체에 적용할 수 있고 안전한 나노 LNP-유전자 편집 기술을 기반으로 대장암 치료제 ‘DREC-21’, 췌장암 치료제 ‘PDAC-11’, 탈모 치료제 ‘HUTERA’를 개발 중이다.
회사의 대장암 치료제는 나노 LNP 캡슐에 단백질 유전자가위를 탑재해 암세포를 찾아 유전자를 편집하는 원리로, 표적 기능과 치료 효과를 확인해 국제학술지 나노리서치(Nano Research)에 보고된 바 있다.
또한, 췌장암 치료제는 하나의 LNP 나노입자에 서로 다른 두 가지 유전자 변이 동시 편집이 가능케 해 치료 효과를 극대화한 결과를 최근 국제 학술지 바이오메터리얼즈(Biomaterials)에 보고했다. 현재 두 개의 암 치료제 모두 비임상시험 독성 평가 진행 중으로, 2023년 완료를 목표하고 있으며 이후 임상시험에 진입할 계획이다.
도포형 탈모 치료제 ‘HUTERA’는 임상 사용 소재로만 이뤄진 개량신약으로, 개발 기간을 줄이고 리스크를 최소화했다. 미세 공기 방울 전달체를 활용해 도포 가능한 제형으로 국부 피부 치료가 가능하며 부작용이 거의 없다. 향후 기타 피부 질환으로도 활용 가능한 플랫폼으로서 특장점이 있다.
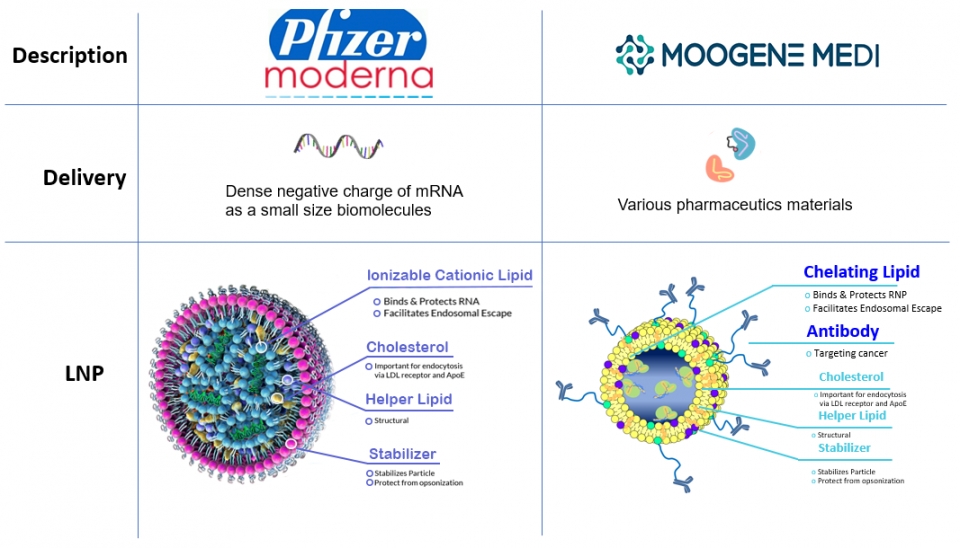
회사 관계자는 “나노 LNP 전달체 기술은 그동안 많은 연구가 진행됐지만, 나노 독성 안전성 연구의 어려움으로 정체돼 있었다. 최근 개발된 화이자, 모더나의 코로나19 백신은 mRNA가 탑재된 LNP로써, 나노 독성이 응급 임상시험 가이드에 의해 빠른 검증을 마쳤다. 이로써 향후 LNP 기술 임상 적용도 속도를 낼 것으로 기대된다”라고 전했다.
이어, “LNP 전문 기업 무진메디는 다양한 약물을 LNP에 탑재해 효과적으로 체내 전달할 수 있는 기술을 보유하고 있다. GMP 제조설비 구축으로 회사 핵심 포트폴리오를 강화하게 됐으며 선제적 준비를 통해 탈모 치료제, 암 치료제 등 주요 제품의 시제품 및 임상시험을 위한 생산에 돌입하고, 빠르게 시장 진입할 것”이라고 설명했다.
㈜무진메디는 앞으로 무균 약물 제제 GMP 생산시설 구축을 통해 기술 파이프라인을 구축하고 임상시험 진행에 속도를 낼 계획이다. 단기적으로 빠른 시장 진입이 예상되는 ‘HUTERA’로 매출 실현을 먼저 달성하고, 이후 회사의 중장기 성장을 견인할 LNP 기반 암 치료제 개발에 집중한다는 방침이다.
[바이오타임즈=박세아 기자] news@biotimes.co.kr


