카이스트 연구팀, 거대 단백질을 블록 쌓듯 조립하는 기술 개발
거대 단백질 구조체는 효율적인 약물 전달, 다양한 백신 개발, 질병 진단에 활용 가능
[바이오타임즈] 단백질은 모든 생물의 몸을 구성하는 고분자 유기물로 수많은 아미노산(Aamino Acid)의 연결체이다.
자연계에는 매우 다양한 특성과 기능을 갖는 단백질이 존재하며, 생명현상을 유지하는 데 핵심적인 역할을 한다. 이러한 단백질 중에는 단량체가 큰 구조체로 조립되었을 때만 정상적 기능을 수행하거나, 단량체와는 아주 다른 특성을 나타내기도 하며, 심각한 질병을 유발할 때도 많다.
이에 거대(초분자) 단백질 구조체들의 조립 기작 이해는 단백질의 기능과 질병의 원인 규명 및 치료제 개발에 중요하다. 또한, 단백질 구조체는 뛰어난 생체 적합도 때문에 생명공학 및 의학 분야에서도 응용 가능성이 높다.
현재 많은 연구진이 자연계에 존재하는 단백질 구조체들의 조립 과정을 모방해 새로운 기능의 단백질 구조체 개발을 연구하고 있다. 주로 나선형 번들 상호 작용, 펩타이드 리간드 상호 작용, 이황화 결합 형성, 화학적 결합, 금속 이온 상호 작용, 자기 결합 단백질 융합과 컴퓨터 설계를 통한 방법 등이 시도됐다. 그러나, 단백질의 구조적 다양성과 서로 다른 특성 및 큰 분자량 때문에 원하는 구조체를 자유자재로 조립하는 것은 아직도 어려운 과제로 남아 있다.
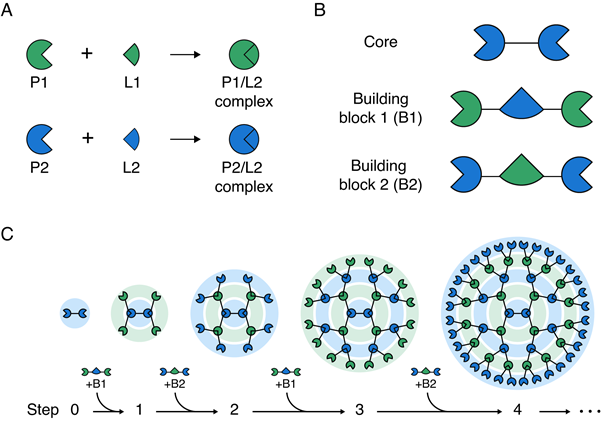
◇카이스트 생명과학과 연구팀, 거대 단백질을 블록 쌓듯 조립하는 기술 개발
이처럼 단백질 구조체 개발이 요원한 가운데, KAIST 생명과학과 김학성 교수와 배진호 박사팀이 거대(초분자) 단백질을 레고 블록 쌓듯 조립할 수 있는 새로운 기술을 개발했다고 19일 밝혔다.
연구팀의 설명으로는 이 방법으로 단백질 구조체의 크기 및 작용기 수를 원하는 대로 조절할 수 있고 메가 달톤(Dalton) 크기의 대칭형 거대 단백질 구조체를 조립할 수 있다. 특히, 거대 단백질 구조체는 효율적인 약물 전달, 다양한 백신 개발, 그리고 질병 진단에 활용될 것으로 기대된다.
김학성 교수 연구팀은 두 종류의 빌딩 블록 단백질을 코어 단백질에 순차적으로 교대로 결합함으로써 간편하게 3차원 구조의 대칭형 거대 단백질 구조체를 조립하는 방법을 개발했다. 즉, 서로 특이적으로 반응하는 두 쌍의 단백질과 리건드(P1/L1 과 P2/L2)를 이용해 코어 단백질에 두 종류의 빌딩 블록을 순차적, 반복적으로 결합함으로써 크기와 작용 기작 수를 조절하면서 메가 달톤 크기를 갖는 단백질 구조체를 쉽게 조립했다.
연구팀은 크기가 27 kDa인 작은 코어 단백질로부터 시작하여 총 4번의 조립 단계를 거쳐 최종적으로 959 kDa의 크기를 갖는 거대 단백질 구조체를 제작했는데, 조립 단계를 증가시키면 보다 큰 단백질 구조체의 제작이 가능하다고 밝혔다.
또한, 각 조립 단계마다 단백질 구조체의 결합가가 2의 배수로 증가하여 구조체의 결합가(Valency) 개수를 쉽게 조절할 수 있고, 다양한 단백질을 쉽게 결합시킬 수 있다고 설명했다.

◇거대 단백질 구조체는 효율적인 약물 전달, 다양한 백신 개발, 질병 진단에 활용 가능
암 표적인 표피생장인자수용체(EGFR)에 특이적인 단백질을 단백질 구조체에 결합한 경우, 구조체 단백질의 특징인 다가 효과(Avidity Effect)로 인해 EGFR에 대한 결합력이 단량체 보다 무려 1,000배 이상 증가했다. 이러한 결합력 증대를 통한 효율적 세포 내 단백질 전달을 위해 박테리아 독소 전달 도메인과 녹색형광단백질 및 식물 유래 독소 단백질인 ‘젤로닌’을 구조체에 결합해 세포 내 단백질 전달이 크게 증대되었으며, 이로 인한 획기적 암 세포 사멸 효과를 확인했다.
이러한 특성은 백신 개발 및 질병 진단에도 응용될 수 있다는 것이 연구팀의 설명이다.
제1 저자인 배진호 박사는 "이번 연구에서 개발된 거대(초분자) 단백질 구조체 조립 기술은 향후, 약물 전달, 백신 개발, 질병 진단 및 바이오센서 등을 포함한 광범위한 분야에서 새로운 플랫폼 기술로 활용될 수 있을 것ˮ이라고 말했다.
이번 연구 성과는 자연계에 존재하는 다양한 구조체들의 조립 및 작용 기작을 이해하는데 기여할 것으로 보인다. 또한, 단백질 구조체는 크기와 다가 효과를 용이하게 조절할 수 있고, 다양한 단백질 Cargo로 기능화할 수 있으며 생체 적합도가 높은 단백질로만 구성되어 있다.
따라서 거대 단백질 구조체 조립 기술은 앞으로 약물 전달, 백신 개발, 질병 진단 및 바이오 센서 등을 포함한 광범위한 분야에서 플랫폼 기술로 활용될 수 있을 것으로 기대된다.
[바이오타임즈=김수진 기자] sjkimcap@biotimes.co.kr


