3차원 생체모사 세포칩의 활용으로 뇌암 치료의 새로운 방향성 제시

[바이오타임즈] 5년 생존율이 7% 미만으로 극복이 힘든 대표적 종양 중 하나인 뇌교모세포종을 치료할 수 있는 약물 플랫폼이 국내 연구진에 의해 개발됐다.
특히 이번 성과는 그간 암세포 자체에 초점을 두었던 뇌암 치료법 연구와 달리, 암과 상호작용하는 환경 내에서 하나의 약물로 다양한 유형의 세포를 동시에 조절함으로써 미세아교세포의 면역항암 치료환경을 개선해 뇌암 치료의 새 지평을 열었다는 평가를 받는다.

◇미세아교세포의 면역항암 치료환경 개선, 뇌암 치료제 약효평가 플랫폼 개발 성공
한국기초과학지원연구원(이하 KBSI) 연구장비개발부 김정아 박사 연구팀과 인천대학교(이하 인천대) 생명공학부 이원종 교수 연구팀은 공동으로 뇌암의 성장과 치료에 있어 중요한 역할을 하는 미세아교세포의 면역 활성 조절과 이를 촉진하기 위한 약물 개발에 활용할 수 있는 약효평가 플랫폼 개발에 성공했다.
연구진이 개발한 작은 세포 칩으로 뇌교모세포종과 뇌 면역세포인 미세아교세포의 상호작용을 들여다보고, 약물의 효능 여부를 판단할 수 있는 플랫폼을 개발함에 따라 난치성 질환인 뇌암 치료제 개발에 탄력이 붙을 것으로 기대된다.
이번 연구는 의약학 분야의 세계적 권위의 학술지인 Theranostics 온라인판[논문명: Inhibition of tumor progression and M2 microglial polarization by extracellular vesicle-mediated microRNA-124 in a 3D microfluidic glioblastoma microenvironment, IF=11.556, JCR 상위 6%, 홍수현(제1저자), 김정아(공동교신저자), 인천대 이원종(공동교신저자)]에 최근 표지논문으로 선정됐다.
뇌교모세포종은 뇌 조직에 풍부하게 존재하는 신경교세포에서 발생하는 뇌암으로, 뇌에서 일차적으로 발생하는 원발성 악성 뇌암의 80%를 차지할 정도로 가장 흔하고 심한 형태의 종양이다. 교모세포종의 정확한 원인은 밝혀지지 않았지만, 바이러스 감염, 방사선 및 발암 물질 노출, 면역 결핍 등에 의한 유전자 손상 및 신경섬유종증과 같은 유전성 증후군이 원인으로 추정된다. 수술, 항암제, 방사선 치료에도, 5년 생존율은 7%도 안 된다.
미세아교세포(Microglia)는 신경 아교 세포의 한 형태로 뇌와 척추 전역에 분포되어 있으며, 뇌에 있는 모든 세포 중의 10~15%를 차지한다. 평소에는 가만히 있다가 처리해야 할 해로운 물질이 생기면 식작용을 하거나 다양한 면역기능을 담당하는 것으로 알려졌다.
최근 이 미세아교세포가 건강한 상태에서 정상적인 뇌의 기능에서 핵심적인 역할을 하는 것으로 밝혀졌다. 뇌 주변의 상황을 감시하며 적재적소에서 뇌 활동을 보호하고 증진하는 항상성 유지와 질병 조절에도 크게 관여한다는 것이다.
또한, 이 세포는 뇌의 보호나 회복은 물론 암의 성장을 저해하는 기능을 하지만, 어떤 환경에서는 정상세포를 공격하거나 암의 성장을 돕는 특징을 보이기도 한다.
이에 공동연구팀은 효과적인 뇌암 치료를 위해서는 뇌암 세포와 미세아교세포 간에 상호작용에 대한 이해를 돕는 플랫폼과 암의 성장을 저해하는 면역 활성을 높일 수 있는 약물의 개발이 매우 중요한 것으로 보고 연구를 진행했다.
◇뇌암의 진행 조절하는 microRNA-124 확인, 3차원 세포칩 안에서 약물 효능 검증
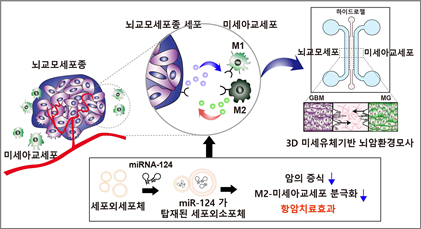
공동연구팀은 뇌암 세포와 미세아교세포의 상호작용을 조절할 수 있는 주요 인자로, 우리 몸의 유전자 발현을 조절하는 microRNA를 세포 외 소포체 안에 탑재하는 방식으로 약물을 제조했다.
세포 외 소포체는 microRNA를 몸 안의 원하는 곳에 안전하게 실어 나를 수 있는 운반체로서, 약물의 유입이 어려운 뇌혈관 장벽까지 통과시킬 수 있는 유용한 약물 전달체다. 엑소좀(Exosome)이라고도 불리며, 세포가 분비하는 지름 50~200nm 크기의 나노 입자로서 세포끼리 주고받는 메시지를 담고 있는 일종의 운반체다.
특히, 많은 종류의 microRNA 중에서도 microRNA-124가 뇌암의 진행을 조절하는 중요한 역할을 할 수 있음을 확인했다. microRNA-124는 교모세포종에서 암의 성장, 이동, 전이를 억제하는 능력과 함께 암의 성장을 돕는 미세아교세포의 활성을 막아내는 역할도 한다.
공동연구팀은 단일세포 차원이 아닌 뇌암과 미세아교세포가 함께 상호작용을 하는 뇌의 환경을 모사하여 만든 3차원 세포 칩 안에서 직접 제조한 약물의 효능을 검증했다.
3차원 세포 칩은 반도체 공정을 통해 주로 제작되는 소형화/집적화된 바이오칩으로서, 세포를 3차원적으로 배양하고 분석할 수 있는 도구다. 의공학/약학 분야에서 생체 모델개발에 널리 쓰이며 동물실험모델을 대체할 수 있을 것으로 기대된다.
KBSI 김정아 박사 연구팀은 3차원 세포 칩을 통해 실제 뇌 환경을 모사한 플랫폼 개발 및 약물 효능 평가를 진행했으며, 인천대 이원종 교수 연구팀은 뇌암과 미세아교세포의 상호작용 환경 조절을 위한 세포 외 소포체 약물 개발에 참여했다.
연구팀의 설명으로는 실제 종양 환경과 기능과 특징이 유사한 3차원 환경에서 세포를 배양하여 약물 후보물질의 독성과 효능을 평가함으로써 정확도를 높일 수 있었다. 또한, 이 플랫폼을 통해 배양된 세포들의 모양과 이동을 관찰·분석할 수 있고, 약물의 효능이 잘 발휘되는지 실시간 확인이 가능하며, 세포 간 상호작용을 통해 나타나는 면역항암 치료 세포의 활성도를 예측할 수 있었다.
연구 결과, miRNA-124가 탑재된 약물이 암세포와 미세아교세포의 항암 기전을 원활히 조절해 NK세포의 침윤을 더 잘 유도할 수 있음을 확인했다. 이로써 miRNA-124에 의해 면역항암효과를 더욱 증진할 수 있을 것으로 예상된다.
KBSI 김정아 박사는 “실제 뇌암의 진행과 치료에 있어 미세아교세포의 역할이 매우 크며, 암과 함께 상호작용하는 환경을 조절함으로써 면역 활성을 높이고 정확한 약효평가를 할 수 있는 생체모사 플랫폼 개발은 매우 중요하다”라면서 “후속 연구로 대량의 이미징 데이터를 높은 효율로 분석할 수 있는 인공지능 기반 이미징 분석법도 개발 중이다”라고 밝혔다.
[바이오타임즈=박세아 기자] news@biotimes.co.kr


