엔도솜 타깃 기전, NOX2를 저해하고 활성화 산소를 억제

[바이오타임즈] 캡슐 형태인 경구용 코로나19 치료제로 개발 중인 압타바이오의 코로나19 치료제 ‘APX-115’가 미국 식품의약국(FDA) 임상 2상 시험계획서(IND)를 승인받았다.
항암치료제 및 당뇨합병증 치료제 개발업체 압타바이오㈜(293780, 대표이사 이수진)는 지난해 12월 코로나19 치료 후보물질 ‘APX-115’의 미국 FDA 임상 2상 시험계획서(IND)를 신청하고, 세계적인 임상시험 수탁 기관인 코방스(COVANCE)와 CRO 계약을 체결한 바 있다.
압타바이오의 ‘APX-115’는 당뇨합병증 치료를 위한 회사의 ‘녹스(NOX) 저해제 발굴 플랫폼’에 기반한 파이프라인 중 하나로, 현재 당뇨병성 신증을 적응증으로 유럽 임상 2상을 진행 중이다.
녹스(NOX)란 체내에 존재하는 7가지 효소로, 활성화 산소(ROS, Reactive Oxygen Species) 생성을 조절해 산화성 스트레스를 조절한다. 해당 효소가 체내에서 과다 생성되면 활성산소량도 비대해져 섬유화와 염증을 유발해 심각한 질병을 초래한다.
‘APX-115’의 해당 기전은 다수의 해외 연구 논문에서 코로나19 치료 효과가 있을 것으로 주목받고 있으며, 회사는 지난해 진행한 세포 실험에서 APX-115가 해당 효과가 있음을 확인하고 연구를 지속해왔다.
학술지 ‘Frontiers in Cellular and Infection Microbiology’에 게재된 미국 시카고 로욜라대학(Loyola University of Chicago) 연구팀의 논문에 따르면, 코로나19 바이러스 복제에는 엔도솜에서 작용하는 NOX가 필수적이며, NOX2로 유도된 활성화 산소는 코로나19로 인한 중증질환인 고혈압, 당뇨병, 심혈관 질환을 유발하며, NOX2가 중요한 바이오마커라고 밝혀졌다.
또한 레독스 바이올로지(Redox Biology) 9월호에서도 이탈리아 로마 사피엔자 대학 (Sapienza University of Rome) 연구팀이 코로나19 환자 체내 NOX2의 상관관계에 대한 논문을 실었다.
해당 논문에 따르면 코로나19 환자는 일반인 대비 NOX2 활성화 수치가 유의성을 인정할 만큼 높게 나타났으며, 특히 중증환자의 경우 더 높은 NOX2 수치를 보였다. 연령, 성별, 체질량 지수, 흡연습관, 동맥 고혈압, 당뇨병, 말초 동맥질환(PAD) 등 심방 세동의 유병률에 대해서는 환자와 대조군 사이의 유의미한 차이가 없었고, 관상 동맥 심장병(CAD), 심부전 및 만성 폐쇄성 폐 질환(COPD)은 코로나19 환자에게서 더 많이 발생했다.
압타바이오 측은 코로나19 환자의 NOX2 활성화 수치가 현저히 높게 나타난다는 연구 결과에 따라 회사의 코로나19 치료제 ‘APX-115’의 효과가 인체 내에서 간접적으로 개념증명(POC, Proof of Concept)이 입증되었다는 분석이다.
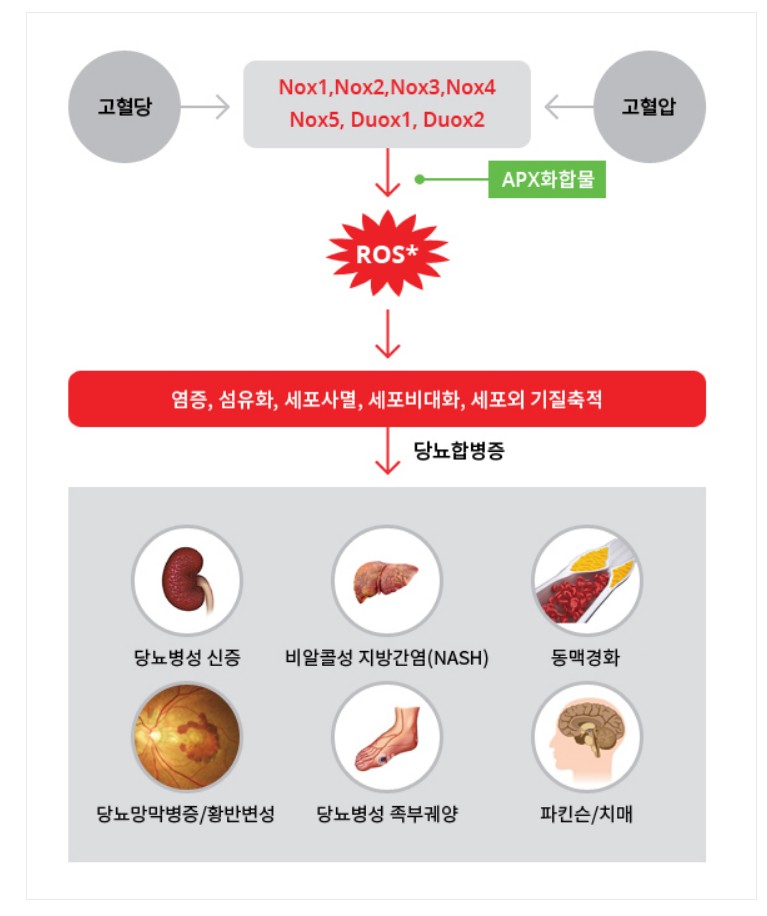
압타바이오의 ‘APX-115’는 엔도솜 타깃으로 하는 기전으로 작용한다. 엔도솜 내 효소 NOX2를 저해하고 활성화 산소를 억제해, 엔도솜을 통한 바이러스 이동을 차단한다. 바이러스 변이를 원천적으로 차단하기 때문에 최근 빠르게 전파되고 있는 변이 바이러스의 대응책이 될 것으로 기대된다.
회사 측은 ‘APX-115’가 기존 적응증에 대해 유럽 임상 1상을 사전 완료하고 안정성 및 부작용 이슈가 없음을 확인했기 때문에 임상 2상으로 빠른 진입이 가능했다고 설명했다.
특히 압타바이오의 코로나19 치료제는 먹는 알약 형태인 ‘경구제’로 개발돼 환자 편의성을 크게 제고했다. 이와 유사한 경구용 치료제로는 최근 임상 1상 시험을 개시한 미국 화이자 ‘프로테아제 억제제’가 대표적이며, 압타바이오는 이보다 한발 앞선 임상 2상을 진행한다.
이번 FDA의 IND 승인에 따라 회사는 미국 내 12개 병원에서 80여 명의 환자를 대상으로 시험에 착수한다. 임상시험 계획에 따르면, 진단 후 14일 이내 환자까지 포함돼 긴급사용 승인을 받은 다른 항바이러스제, 항체치료제보다 넓은 범위의 환자가 선정됐다.
다른 긴급사용승인 항바이러스제, 항체치료제가 진단된 지 얼마 안 된 환자를 대상으로 시험을 진행하는 것과 달리, 보다 넓은 범위의 환자까지 시험을 진행함으로써 바이러스 증상 외에 염증 및 섬유화 등 합병증에 대한 치료 효과 또한 검증할 예정이다.
압타바이오 측은 NOX 조절이 코로나19 환자 임상 치료에서 핵심이 될 것이며, 중증질환 환자에게도 새로운 표적 치료법이 될 것으로 기대한다. 회사는 세계적인 임상시험 수탁 기관인 코방스(COVANCE)와 CRO 계약을 체결한 만큼, 그들의 글로벌 임상 수행 경험과 노하우를 활용해 미국 FDA 임상 2상 시험에 속도를 내고, 성공적인 결과 도출을 위해 최선을 다할 계획이다.
압타바이오 관계자는 “FDA 임상2상 결과에 따라 치료적 확증 임상시험을 완료하고 긴급사용 승인 등 신속한 절차를 시도할 계획”이라며 “회사의 치료제가 글로벌 임상을 진행함에 따라, 치료제 개발이 완료되면 전 세계 보건에 이바지할 수 있을 것이라 기대된다”고 밝혔다.
[바이오타임즈=강철현 기자] kch@biotimes.co.kr


