연구부터 임상, 생산까지 보유한 기업으로 항암 면역치료제 플랫폼 개발

[바이오타임즈] 항암면역치료제 개발 전문기업 박셀바이오(323990, 대표 이준행·이제중)의 주가가 강세를 보이고 있다. 2거래일 연속 하락세를 딛고 크게 반등하는 모양새다.
박셀바이오는 12일 낮 1시 27분 현재 전 거래일 대비 7.68% 오른 10만 1,000원에 거래되고 있다.
급등 배경에는 최근 세포배양 특허를 취득했다는 소식이 호재로 작용하고 있는 것으로 풀이된다.
박셀바이오는 지난 8일 공시를 통해 ‘OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양 방법‘과 관련한 특허를 취득했다고 밝혔다.
회사 관계자는 “OX40L을 발현하는 배양보조세포를 말초혈액 단핵구와 함께 공배양시키면 일반적인 K562 세포주를 배양보조세포로 이용하는 방법과 비교해 높은 수준의 순도 및 증폭률로 자연살해세포를 증식시킬 수 있다”고 설명했다.
이어 “자연살해세포를 이용한 다양한 면역세포 치료 분야에서 치료 효율 및 치료 효능을 획기적으로 증진시킬 수 있을 것”이라고 덧붙였다.
박셀바이오는 지난 2010년 전남대학교 의과대학 및 임상 백신 연구개발사업단에서 분사해 창업한 항암 면역치료제 전문 바이오 기업이다. 국내 면역학 권위자인 이준행 대표이사와 혈액암 권위자인 이제중 CMO(최고의료책임자) 등 정상급 연구진을 중심으로 자연살해(NK) 세포와 수지상세포(DC)를 활용한 항암 면역치료 플랫폼을 개발하고 있다.
연구성과와 기술성을 인정받아 지난해 9월 코스닥에 상장했다.
박셀바이오는 항암 면역치료제 기초 연구부터 임상 설계, 임상시험, 생산이 가능한 연구소와 설비를 갖추고 있다.
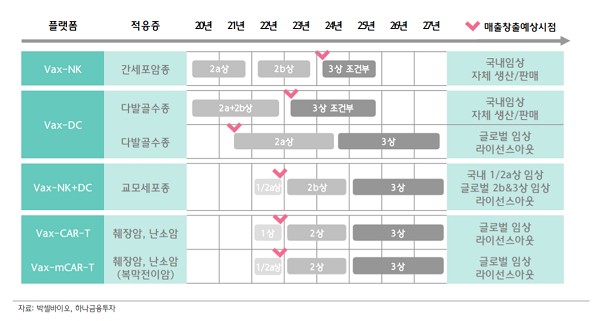
현재 핵심 파이프라인(신약후보 물질)은 2개로, 자가 NK세포를 활용한 간암 치료제(‘VAX-NK’)의 임상 2상과 자가 수지상세포(dendritic cell, DC)를 활용한 다발골수종 치료제(‘VAX-DC’)의 임상 2상을 진행 중이다. 강력한 차세대 항암 면역치료제로 꼽히는 CAR-T 치료제도 동물실험을 통해 안전성과 효과를 확인 중이다.
특히 NK세포를 활용한 항암 면역치료 플랫폼(Vax-NK)이 기존 NK세포 치료제와 비교해 임상 진행이 빠르며, 진행성 간암 환자를 대상으로 수행한 임상 1상 중 72.7%의 환자에게서 객관적 반응이 관찰됐고 80%가 넘는 환자에게 질병 조절능력이 보였다고 회사 측은 설명했다.
박셀바이오사의 면역세포 치료제는 대부분 자가 방식으로 병원에서 시술이 이루어진다는 점에서 간세포암 환자 대상의 Vax-NK는 국내에서 자체 생산/판매될 것으로 예상하므로, 임상 2b상완료 이후 조건부 승인을 통해 2024년 상업화가 가능할 것으로 기대된다는 의견이다.
아울러 다발골수종 치료제 Vax-DC와 교모세포종 치료제 Vax-NK+DC와 췌장암, 난소암치료제 VaxCAR-T 등은 글로벌 임상을 통한 라이선스 아웃(기술수출)으로 오는 2022년경부터 매출 발생을 전망했다.
이와 함께 세계 최초로 개발 중인 박스루킨-15 반려동물 전용 항암 면역 치료제가 조기 상업화가 가능할 것으로 기대되고 있다.
다만 최근 개발 중인 반려동물 항암제 ‘박스루킨25’의 품목허가 과정에서 보완요청을 받았다는 소식에 주가가 하락하기도 했다.
박스루킨은 세계 최초 반려견 전용 항암면역치료 사이토카인 제제다. 지난해 10월 박셀바이오는 박스루킨에 대해 품목허가 서류를 공식접수했다.
회사 측은 “2월 25일자로 박스루킨15 품목허가에 대해 농림축산검역본부(검역본부)로부터 보완요청을 받았다”고 홈페이지를 통해 밝혔다. 생산시설 변경에 따른 안정성 시험, 비교 동등성 시험 자료에 대한 추가 제출을 요청받은 것으로, 이는 효능이나 제조공정 자체에 대한 지적사항이 아니라는 설명이다.
이에 보완요청 내용을 면밀히 검토한바, 대응자료 작성에 큰 애로가 없을 것으로 판단을 내려 가장 빠른 시간 내에 대응자료를 제출하겠다는 입장이다.
[바이오타임즈=강철현 기자] kch@biotimes.co.kr


